A gravidez e a completa reestruturação do epitélio intestinal!
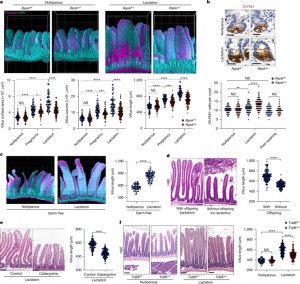
Legenda: No painel a, uma reconstrução 3D representativa do intestino delgado de camundongos controles e caRANKvil-Tg com 3 semanas de idade, com espaçamento da grade de 200 µm, revelou diferenças significativas na morfologia. Nos camundongos caRANKvil-Tg (n = 7, 145 vilos analisados) foram observados aumentos no comprimento, volume e áreas superficiais dos vilos em comparação aos controles (n = 6, 126 vilos). No painel b, imunomarcação de OLFM4 nos intestinos delgados de camundongos controles e caRANKvil-Tg em diferentes idades mostrou uma diminuição no número de células OLFM4+ por cripta nos camundongos transgênicos. Em 3 semanas, os controles apresentaram 234 criptas, enquanto os caRANKvil-Tg apresentaram 205; em 4 semanas, foram observadas 162 criptas nos controles e 110 nos caRANKvil-Tg; e em 5–8 semanas, 203 criptas nos controles contra 178 nos transgênicos. No painel c, uma reconstrução 3D dos intestinos delgados de camundongos controles e caRANKvil-Tg com 5–8 semanas de idade confirmou o aumento no comprimento, volume e área superficial dos vilos nos camundongos caRANKvil-Tg (n = 5, 65 vilos) em comparação aos controles (n = 4, 47 vilos). No painel d, a imunomarcação de OLFM4 no intestino delgado de camundongos caRANKvil-Tg;Traf6^fl/+ (n = 3) e caRANKvil-Tg;Traf6^fl/fl (n = 5) de 8 semanas evidenciou diferenças significativas. No painel e, foram quantificados o número de células OLFM4+ por cripta e o comprimento dos vilos nos camundongos caRANKvil-Tg;Traf6^fl/+ (n = 3, 172 criptas e 40 vilos) e caRANKvil-Tg;Traf6^fl/fl (n = 5, 299 criptas e 167 vilos). No painel f, imagens macroscópicas dos intestinos delgados de camundongos Apc^min/+ e caRANKvil-Tg;Apc^min/+ destacaram diferenças visíveis na morfologia, com escalas de 7,5 mm. No painel g, a razão de tumoroides cultivados sem (controle) ou com rmRANKL (50 ng/ml) foi normalizada em relação ao grupo controle, com dados combinados de dois experimentos independentes (n = 4 para cada condição). Imagens representativas de tumoroides de camundongos Apc^min/+ em diferentes passagens (0, 1 e 2), cultivados na ausência ou presença de rmRANKL, mostraram alterações no tamanho e crescimento. Os dados de todos os painéis são apresentados como média ± desvio padrão. A análise estatística foi realizada com testes t de Student de duas caudas (painéis a, c, e e g) e ANOVA de uma via com teste post hoc de Tukey (painel b), com significância indicada como *P < 0,05 e NS para não significativo.
Creditos da imagem: Onji et al, 2024
Durante a gravidez e a lactação, os organismos de mamíferos passam por profundas adaptações fisiológicas para garantir a saúde da mãe e o desenvolvimento ideal da prole. Uma dessas adaptações, revelada por um estudo inovador publicado na Nature, é a expansão do epitélio intestinal, um processo mediado pelo sistema molecular RANK–RANKL. Essa remodelação do intestino, crucial para atender às demandas nutricionais elevadas, representa um marco na evolução dos mamíferos.
O estudo mostrou que, durante a gravidez, os vilos intestinais se alongam e a área da superfície intestinal aumenta significativamente, otimizando a absorção de nutrientes. Esse processo é controlado pelo receptor RANK, expresso no epitélio intestinal, que interage com seu ligante RANKL. Essa interação protege as células epiteliais contra a apoptose, regula o nicho de células-tronco intestinais e ativa a sinalização BMP, essencial para a diferenciação celular e para o crescimento das estruturas intestinais. Inicialmente, a ativação do RANKL promove a expansão das células-tronco intestinais, mas a estimulação prolongada pode levar à exaustão dessas células e à disfunção do epitélio.
A importância desse mecanismo vai além da saúde da mãe. Filhotes nascidos de fêmeas deficientes em RANK no epitélio intestinal apresentaram redução de peso ao nascimento e durante o período de amamentação, além de maior propensão à intolerância à glicose quando submetidos a dietas ricas em gorduras na vida adulta. Esses resultados indicam que a expansão do epitélio intestinal durante a gravidez é essencial não apenas para suprir as necessidades nutricionais imediatas, mas também para garantir a saúde metabólica a longo prazo da prole.
Outro aspecto marcante desse processo é sua reversibilidade. Após o término da lactação, o epitélio intestinal retorna ao seu estado original, um efeito mediado por hormônios reprodutivos, como a prolactina, que intensificam a expressão de RANKL durante a gravidez e a amamentação. Essa plasticidade demonstra como o intestino se adapta às demandas reprodutivas de forma eficiente e controlada.
Os achados do estudo também têm implicações clínicas. A sinalização RANK–RANKL desempenha um papel central na regulação do epitélio intestinal em humanos, conforme demonstrado em experimentos com organoides intestinais. Isso sugere que alterações nesse sistema podem estar associadas a doenças como câncer intestinal e outras disfunções metabólicas, abrindo caminhos para novas abordagens terapêuticas.
Em síntese, o estudo sobre o eixo RANK–RANKL revela como a biologia reprodutiva molda a função intestinal para otimizar a nutrição materna e a saúde da prole. Essa descoberta destaca não apenas a complexidade das adaptações maternas, mas também sua relevância para a saúde intergeracional, reforçando a importância de um entendimento profundo das adaptações fisiológicas na reprodução.
RANK drives structured intestinal epithelial expansion during pregnancy
RANK drives structured intestinal epithelial expansion during pregnancy